
Нуклони. Заряд і масове число. Ізотопи
|
|
До 1932 року чіткого розуміння структури ядра не було. Були різні варіанти (ядро складалось із протонів та електронів; тільки з протонів та ін.), але розрахунки показали, що в дійсності ядро було набагато важче.
У 1932 році англійський вчений Д. Чедвік відкрив нейтрон. При бомбардуванні берилію α-частинками був одержаний ізотоп вуглецю. Було виявлено якесь сильне випромінювання, нейтральне, з великою проникною здатністю. Це були окремі частинки, які згодом назвали нейтронами:
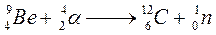 .
.
Після відкриття нейтрону радянський фізик Іванов і незалежно від нього Гейзенберг запропонували протонно-нейтронну модель ядра. Ядро складалося з протонів і нейтронів. Але при цьому не було згадано про те, яким чином розташовуються в ядрі протони і нейтрони.
Протон (р) – позитивно заряджена частинка. Заряд (q), маса (m), радіус (r), час життя (t), магнітний момент (р), спін (s), наведені нижче:
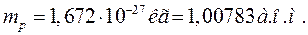 (
( 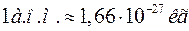 ),
),
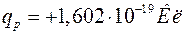 ,
,
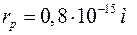 ,
,
 ,
,
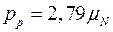 ,
,
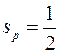 .
.
У кожному ядрі мало б міститися стільки протонів, скільки електронів в атомі, і це забезпечувало електронейтральність атома.
Для опису магнітних характеристик нуклонів і ядер користуються ядерним магнетоном (у 1836 разів меншим від магнетону Бора):
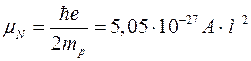 .
.
Нейтрон (n) – нейтральна частинка. Характеристики наведені нижче:
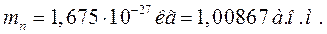 ,
,
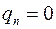 ,
,
 ,
,
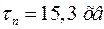 ,
,
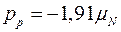 ,
,
 .
.
Хоча нейтрон позбавлений заряду, все ж він має магнітний момент, що дорівнює – 1,91 ядерних магнетонів. Знак мінус тут вказує, що за напрямом магнітний момент протилежний спіну нейтрона.
У вільному стані нейтрон нестійкий і самовільно розпадається (період піврозпаду Т = 12 хв): випромінюючи β-частинку і антинейтрино, він перетворюється у протон.
Властивості ядра
Число, яке є найближчим до атомної маси (таблиця Менделєєва) в атомних одиницях маси називається масовим числом (А). Пишеться у верхньому індексі.
Зарядне число визначає заряд ядра в одиницях заряду електрона, тобто показує кількість протонів в ядрі (та кількість електронів в атомі). Пишеться у нижньому індексі:
 .
.
Протони і нейтрони називають ще нуклонами.
Масове число – число нуклонів у ядрі:
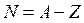 (кількість нейтронів).
(кількість нейтронів).
Протонно-нейтронна теорія будови ядра добре узгоджується з дослідними даними.
Як було показано, маси протона і нейтрона дуже мало відрізняються від атомної одиниці маси. Тому відповідно до системи елементів Д. І. Менделєєва, за протонно-нейтронною теорією, порядковий номер елемента Z визначає число протонів в ядрі атома, а масове число А – сумарну кількість протонів і нейтронів ядра; (А – Z) – число нейтронів у ядрі. Як складові частинки ядра протони і нейтрони виявляють у численних ядерних реакціях поділу і синтезу.
Звичайно, в самовільних і штучних поділах ядер спостерігаються також потоки електронів, позитронів, мезонів, нейтрино і антинейтрино. Маса β-частинки (електрона або позитрона) в 1836 разів менша від маси нуклона. Мезони – позитивні, негативні і нульові частинки за величиною маси займають проміжне місце між β-частинками і нуклонами; час життя їх дуже малий (мільйонні і менші долі секунди). Нейтрино і антинейтрино – елементарні частинки, масу спокою їх беруть такою, що дорівнює нулю. Проте електрони, позитрони і мезони не можуть бути складовими частинками ядра. Ці легкі частинки не можуть бути локалізованими в такому малому об'ємі, яким є ядро з радіусом 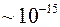 м. Для доведення цього обчислимо енергію електричної взаємодії, наприклад, електрона з позитроном чи протоном в ядрі:
м. Для доведення цього обчислимо енергію електричної взаємодії, наприклад, електрона з позитроном чи протоном в ядрі:
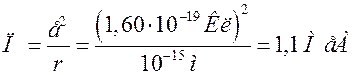 .
.
і порівняємо її з власною енергією електрона:
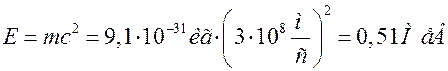 .
.
Оскільки енергія зовнішньої взаємодії перевищує власну енергію електрона, то він не може існувати і зберігати свою індивідуальність, в умовах ядра він буде зруйнований. Зовсім інше становище у нуклонів, їхня власна енергія понад 900 МеВ, тому в ядрі вони можуть існувати і зберігати свою індивідуальність.
Різними методами встановлено, що радіус ядра з достатньою точністю можна визначати за формулою:
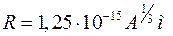 ,
,
де А – число нуклонів у ядрі.
Визначивши об'єм ядра, маємо:
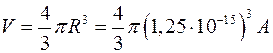 .
.
Об'єм ядра прямопропорційний числу нуклонів. Інакше кажучи, в усіх ядрах на один нуклон припадає однаковий об'єм; цим самим ядра уподібнюються до нестисливої рідини. Густина ядерної речовини:
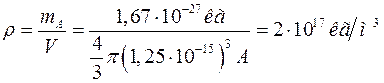 .
.
Значна густина ядерної речовини є також ознакою величезних сил взаємодій між нуклонами.
Легкі частинки випромінюються з ядер у процесі переходів їх з одного стану в інший.
Існують ядра, які мають однакове зарядове число, але різне масове число. Такі елементи повинні знаходитись в одній клітинці періодичної системи.
Елементи, які мають однакове зарядне число і різне масове число, називаються ізотопами:
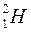 – дейтерій,
– дейтерій, 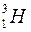 – тритій.
– тритій.
|
© 2013 wikipage.com.ua - Дякуємо за посилання на wikipage.com.ua | Контакти |